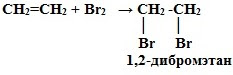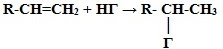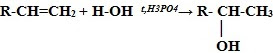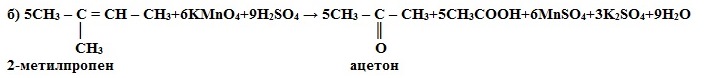Персональный сайт
Ростовцевой Ларисы Геннадьевны
учителя химии МБОУ Боханской СОШ № 2
|
Меню сайта
Наш опрос
Погода
|
Алкены: физические и химические свойстваАлкены: физические и химические свойстваФизические свойства Первые три представителя гомологического ряда алкенов (этилен, пропилен и бутилен) — газы, начиная с C5H10 (амилен, или пентен-1) — жидкости, а с С18Н36 — твердые вещества. С увеличением молекулярной массы повышаются температуры плавления и кипения. Алкены нормального строения кипят при более высокой температуре, чем их изомеры, имеющие изостроение. Температуры кипения цис-изомеров выше, чем транс-изомеров, а температуры плавления — наоборот. Алкены плохо растворимы в воде (однако лучше, чем соответствующие алканы), но хорошо — в органических растворителях. Этилен и пропилен горят коптящим пламенем. Таблица 1. Физические свойства некоторых алкенов
Химические свойства алкенов Для алкенов наиболее типичными являются реакции присоединения. В реакциях присоединения двойная связь выступает как донор электронов, поэтому для алкенов характерны реакции электрофильного присоединения. 1. Реакции присоединения 1. Гидрирование (гидрогенизация – взаимодействие с водородом): CnH2n + H2 t, Ni → CnH2n+2 2. Галогенирование (взаимодействие с галогенами): CnH2n + Г2 → СnH2nГ2
Это качественная реакция алкенов – бромная вода Br2 (бурая жидкость) обесцвечивается. Опыт: “Взаимодействие этилена с бромной водой” 3. Гидрогалогенирование* (взаимодействие с галогенводородами):
4. Гидратация* (присоединение молекул воды): CH2=CH2 + H2O t,H3PO4→ CH3-CH2-OH (этанол – этиловый спирт) * Присоединение галогенводородов и воды к несимметричным алкенам происходит поправилу Марковникова В.В. Присоединение водорода происходит к наиболее гидрированному атому углерода при двойной углерод-углеродной связи. Исключения!!! 1) Если в алкене присутствует электроноакцепторный заместитель, т.е. группа, способная оттягивать на себя электронную плотность: F3C ← CH=CH2 + H-Br → F3C - CH2 - CH2(Br) 1,1,1- трифтор-3-бромпропан 2) Присоединение в присутствии Н2О2 (эффект Хараша) или органической перекиси (R-O-O-R ): СH3-CH=CH2 + H-Br Н2О2 → H3C - CH2 - CH2(Br) 5. Реакции полимеризации: nCH2=CH2 t, p, kat-TiCl4, Al(C2H5)3 → (-CH2-CH2-)n мономер - этилен полимер – полиэтилен
2. Реакции окисления 1. Горение: CnH2n + 3n/2O2 t, p, kat → nCO2 + nH2O + Q (пламя ярко светящее) Опыт: “Горение этилена” Частичное окисление этилена
2. Окисление перманганатом калия (р. Вагнера) в нейтральной среде – это качественная реакция алкенов, розовый раствор марганцовки обесцвечивается.
Влияние среды на характер продуктов реакций окисления 1) Окисление в кислой среде при нагревании идёт до а) карбоновых кислот; б) кетонов (если атом углерода при двойной связи содержит два заместителя); в) углекислого газа (если двойная связь на конце молекулы, то образуется муравьиная кислота, которая легко окисляется до CO2): а) 5CH3-CH=CH-CH3 + 8KMnO4 + 12H2SO4 → 10CH3COOH + 8MnSO4 +4K2SO4 + 12H2O
в) CH3 – CH2 – CH = CH2 + 2KMnO4 + 3H2SO4 → CH3CH2COOH + CO2 + 2MnSO4 + K2SO4 + 4H2O 2) Окисление в нейтральной или слабощелочной среде на холоде (см. выше) Опыт: “Взаимодействие этилена с раствором перманганата калия” Тренажеры Тренажер №1: “Уравнения реакций, характеризующие химические свойства этилена и пропилена” Тренажер №2: “Химические свойства алкенов” Тренажер №3: “Химические свойства алкенов (расчетные задачи)” |
Поиск
Архив записей
Друзья сайта
Статистика
Онлайн всего: 1 Гостей: 1 Пользователей: 0 |
||||||||||||||||||||||||||||||||||||||||||||||||||||