Персональный сайт
Ростовцевой Ларисы Геннадьевны
учителя химии МБОУ Боханской СОШ № 2
|
Меню сайта
Наш опрос
Погода
|
Предельные одноатомные спирты: строение, изомерия, номенклатура, физические свойстваПредельные одноатомные спирты: строение, изомерия, номенклатура, физические свойства. Водородная связь. Физиологическое действие спиртов на организм человека
Рис. а) этанол б) метанол Спиртами называют соединения, содержащие одну или несколько гидроксильных групп, непосредственно связанных с углеводородным радикалом. I. Классификация спиртов Спирты классифицируют по различным структурным признакам. 1. По числу гидроксильных групп
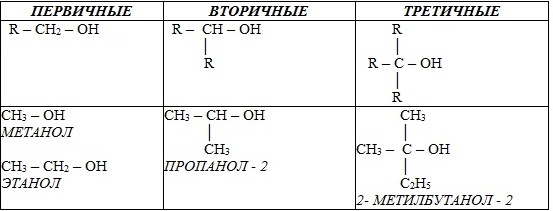
Современное название многоатомных спиртов - полиолы (диолы, триолы и т.д). Примеры: двухатомный спирт – этиленгликоль (этандиол): HO–СH2–CH2–OH трехатомный спирт – глицерин (пропантриол-1,2,3): HO–СH2–СН(ОН)–CH2–OH Двухатомные спирты с двумя ОН-группами при одном и том же атоме углерода R–CH(OH)2 неустойчивы и, отщепляя воду, сразу же превращаются в альдегиды R–CH=O. Спирты R–C(OH)3 не существуют. 2. В зависимости от того, с каким атомом углерода (первичным, вторичным или третичным) связана гидроксигруппа, различают спирты
Например:
В многоатомных спиртах различают первично-, вторично- и третичноспиртовые группы. Например, молекула трехатомного спирта глицерина содержит две первичноспиртовые (HO–СH2–) и одну вторичноспиртовую (-СН(ОН)–) группы. 3. По строению радикалов, связанных с атомом кислорода
Непредельные спирты с ОН-группой при атоме углерода, соединенном с другим атомом двойной связью, очень неустойчивы и сразу же изомеризуются в альдегиды или кетоны. Например, виниловый спирт CH2=CH–OH превращается в уксусный альдегид CH3–CH=O Гомологический ряд предельных одноатомных спиртов Предельные одноатомные спирты – кислородсодержащие органические вещества, производные предельных углеводородов, в которых один атом водорода замещён на функциональную группу (-OH) Общая формула: CnH2n+1OH или ROH или CnH2n+2O
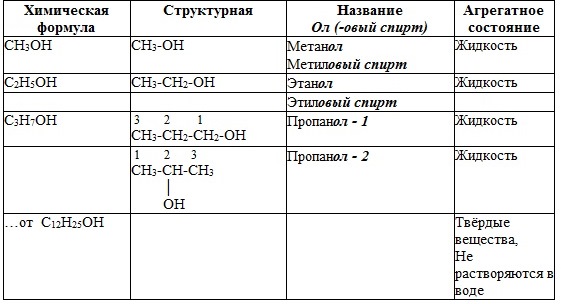
Структурные формулы предельных одноатомных спиртов Номенклатура спиртов Систематические названия даются по названию углеводорода с добавлением суффикса -ол и цифры, указывающей положение гидроксигруппы (если это необходимо). Например:
Нумерация ведется от ближайшего к ОН-группе конца цепи. Цифра, отражающая местоположение ОН-группы, в русском языке обычно ставится после суффикса "ол".
По другому способу (радикально-функциональная номенклатура) названия спиртов производят от названий радикалов с добавлением слова "спирт". В соответствии с этим способом приведенные выше соединения называют: метиловый спирт, этиловый спирт, н-пропиловый спирт СН3-СН2-СН2-ОН, изопропиловый спирт СН3-СН(ОН)-СН3. Изомерия спиртов 1. Cтруктурная изомерия 1) Изомерия положения ОН-группы (начиная с С3)
2) Изомерия углеродного скелета (начиная с С4)
2. Межклассовая изомерия с простыми эфирами этиловый спирт СН3CH2–OH и диметиловый эфир CH3–O–CH3 3. Пространственная изомерия – оптическая Например, бутанол-2 СH3CH(OH)СH2CH3, в молекуле которого второй атом углерода (выделен цветом) связан с четырьмя различными заместителями, существует в форме двух оптических изомеров. Строение спиртов Строение самого простого спирта — метилового (метанола) — можно представить формулами: Из электронной формулы видно, что кислород в молекуле спирта имеет две неподеленные электронные пары. Свойства спиртов и фенолов определяются строением гидроксильной группы, характером ее химических связей, строением углеводородных радикалов и их взаимным влиянием. Связи О–Н и С–О – полярные ковалентные. Это следует из различий в электроотрицательности кислорода (3,5), водорода (2,1) и углерода (2,4). Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода:
Взаимное влияние атомов в молекуле этанола  Атому кислорода в спиртах свойственна sp3-гибридизация. В образовании его связей с атомами C и H участвуют две 2sp3-атомные орбитали, валентный угол C–О–H близок к тетраэдрическому (около 108°). Каждая из двух других 2 sp3-орбиталей кислорода занята неподеленной парой электронов. Подвижность атома водорода в гидроксильной группе спирта несколько меньше, чем в воде. Более "кислым" в ряду одноатомных предельных спиртов будет метиловый (метанол). Физические свойства МЕТАНОЛ (древесный спирт) – жидкость (tкип=64,5; tпл=-98; ρ = 0,793г/см3), с запахом алкоголя, хорошо растворяется в воде. Ядовит – вызывает слепоту, смерть наступает от паралича верхних дыхательных путей. ЭТАНОЛ (винный спирт) – б/цв жидкость, с запахом спирта, хорошо смешивается с водой. Первые представители гомологического ряда спиртов — жидкости, высшие — твердые вещества. Метанол и этанол смешиваются с водой в любых соотношениях. С ростом молекулярной массы растворимость спиртов в воде падает. Высшие спирты практически нерастворимы в воде. Видео-опыт: “Физические свойства спиртов” Особенности строения спиртов – спирты образуют водородные связи (обозначают точками) за счёт функциональной группы (-ОН) а) Водородная связь между молекулами спиртов  б) Водородная связь между молекулами спирта и воды
Вывод:
1) В результате у всех спиртов более высокая температура кипения, чем у соответствующих углеводородов, например, Т. кип. этанола +78° С, а Т. кип. этана –88,63° С; Т. кип. бутанола и бутана соответственно +117,4° С и –0,5° С. 2) Способность спиртов образовывать межмолекулярные водородные связи не только влияет на их температуры кипения, но и увеличивает их растворимость в воде. Все алканы нерастворимы в воде, а низкомолекулярные спирты (метиловый, этиловый, н-пропиловый и изопропиловый) растворяются в воде неограниченно. 3) Отсутствие газов в гомологическом ряду предельных одноатомных спиртов. Физиологическое действие спиртов на организм человека Тренажеры Тренажер №1: “Изомерия предельных одноатомных спиртов” Тренажер №2: “Классификация спиртов” Тренажер №3: “Номенклатура предельных одноатомных спиртов” |
Поиск
Архив записей
Друзья сайта
Статистика
Онлайн всего: 1 Гостей: 1 Пользователей: 0 |
||||||||||||