Персональный сайт
Ростовцевой Ларисы Геннадьевны
учителя химии МБОУ Боханской СОШ № 2
|
Меню сайта
Наш опрос
Погода
|
Бензол: свойства, получение и применениеБензол: физические и химические свойства, получение и применениеФизические свойства Видео-опыт: “Изучение физических свойств бензола” Бензол и его ближайшие гомологи – бесцветные жидкости со специфическим запахом. Ароматические углеводороды легче воды и в ней не растворяются, однако легко растворяются в органических растворителях – спирте, эфире, ацетоне. Бензол и его гомологи сами являются хорошими растворителями для многих органических веществ. Все арены горят коптящим пламенем ввиду высокого содержания углерода в их молекулах. Таблица. Физические свойства некоторых аренов
Бензол – легкокипящая (tкип = 80,1°С), бесцветная жидкость, не растворяется в воде Внимание! Бензол – яд, действует на почки, изменяет формулу крови (при длительном воздействии), может нарушать структуру хромосом. Большинство ароматических углеводородов опасны для жизни, токсичны. Получение аренов (бензола и его гомологов) 1. В лаборатории 1. Сплавление солей бензойной кислоты с твёрдыми щелочами C6H5-COONa + NaOH t → C6H6 + Na2CO3 бензоат натрия 2. Реакция Вюрца-Фиттинга: (здесь Г – галоген) С6H5-Г + 2Na + R-Г → C6H5-R + 2NaГ С6H5-Cl + 2Na + CH3-Cl → C6H5-CH3 + 2NaCl 2. В промышленности
1. Дегидроциклизацией алканов с числом атомов углерода больше 6: C6H14 t, kat→ C6H6 + 4H2
2. Тримеризация ацетилена (только для бензола) – реакция Зелинского 3С2H2 600°C, акт. уголь → C6H6
3. Дегидрированием циклогексана и его гомологов Советский академик Николай Дмитриевич Зелинский установил, что бензол образуется из циклогексана (дегидрирование циклоалканов) C6H12 t, kat→ C6H6 + 3H2
C6H11-CH3 t, kat→ C6H5-CH3 + 3H2 метилциклогексан толуол 4. Алкилирование бензола (получение гомологов бензола) – реакция Фриделя-Крафтса C6H6 + C2H5-Cl t, AlCl3→ C6H5-C2H5 + HCl хлорэтан этилбензол
Химические свойства аренов I. Реакции окисления 1. Горение (коптящее пламя): Видео-опыт: “Горение бензола” 2C6H6 + 15O2 t → 12CO2 + 6H2O + Q 2. Бензол при обычных условиях не обесцвечивает бромную воду и водный раствор марганцовки Видео-опыт: “Изучение отношения бензола к бромной воде и раствору перманганата калия” 3. Гомологи бензола окисляются перманганатом калия (обесцвечивают марганцовку): а) в кислой среде до бензойной кислоты При действии на гомологи бензола перманганата калия и других сильных окислителей боковые цепи окисляются. Какой бы сложной ни была цепь заместителя, она разрушается, за исключением a -атома углерода, который окисляется в карбоксильную группу. Гомологи бензола с одной боковой цепью дают бензойную кислоту:
Гомологи, содержащие две боковые цепи, дают двухосновные кислоты:
5C6H5-C2H5 + 12KMnO4 + 18H2SO4 → 5C6H5COOH + 5CO2 + 6K2SO4 + 12MnSO4+28H2O 5C6H5-CH3 + 6KMnO4 + 9H2SO4 → 5C6H5COOH + 3K2SO4 + 6MnSO4 +14H2O Упрощённо: C6H5-CH3 + 3O KMnO4 → C6H5COOH + H2O б) в нейтральной и слабощелочной до солей бензойной кислоты C6H5-CH3 + 2KMnO4 → C6H5COOК + KОН + 2MnO2 + H2O II. Реакции присоединения (труднее, чем у алкенов) 1. Галогенирование C6H6 +3Cl2 hν → C6H6Cl6 (гексахлорциклогексан - гексахлоран)
Видео-опыт: “Хлорирование бензола (получение гексахлорана)” 2. Гидрирование C6H6 + 3H2 t,Pt или Ni → C6H12 (циклогексан) 3. Полимеризация III. Реакции замещения – ионный механизм (легче, чем у алканов) 1. Галогенирование a) бензола C6H6 + Cl2 AlCl3→ C6H5-Cl + HCl (хлорбензол)
C6H6 + 6Cl2 t ,AlCl3→ C6Cl6 + 6HCl (гексахлорбензол) C6H6 + Br2 t,FeCl3→ C6H5-Br + HBr (бромбензол)
Видео-опыт: “Бромирование бензола” б) гомологов бензола при облучении или нагревании По химическим свойствам алкильные радикалы подобны алканам. Атомы водорода в них замещаются на галоген по свободно-радикальному механизму. Поэтому в отсутствие катализатора при нагревании или УФ-облучении идет радикальная реакция замещения в боковой цепи. Влияние бензольного кольца на алкильные заместители приводит к тому, что замещается всегда атом водорода у атома углерода, непосредственно связанного с бензольным кольцом (a -атома углерода). 1) C6H5-CH3 + Cl2 hν → C6H5-CH2-Cl + HCl 2) в) гомологов бензола в присутствии катализатора C6H5-CH3 + Cl2 AlCl3→ (смесь орта, пара производных) + HCl 2. Нитрование (с азотной кислотой) C6H6 + HO-NO2 t, H2SO4→ C6H5-NO2 + H2O нитробензол - запах миндаля!
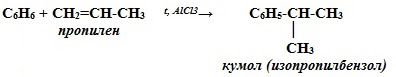
Видео-опыт: “Нитрование бензола” C6H5-CH3 + 3HO-NO2 t, H2SO4→ СH3-C6H2(NO2)3 + 3H2O 2,4,6-тринитротолуол (тол, тротил) Применение бензола и его гомологов Бензол C6H6 – хороший растворитель. Бензол в качестве добавки улучшает качество моторного топлива. Служит сырьем для получения многих ароматических органических соединений – нитробензола C6H5NO2 (растворитель, из него получают анилин), хлорбензола C6H5Cl, фенола C6H5OH, стирола и т.д. Толуол C6H5–CH3 – растворитель, используется при производстве красителей, лекарственных и взрывчатых веществ (тротил (тол), или 2,4,6-тринитротолуол ТНТ). Ксилолы C6H4(CH3)2. Технический ксилол – смесь трех изомеров (орто-, мета- и пара-ксилолов) – применяется в качестве растворителя и исходного продукта для синтеза многих органических соединений. Изопропилбензол C6H5–CH(CH3)2 служит для получения фенола и ацетона. Хлорпроизводные бензола используют для защиты растений. Так, продукт замещения в бензоле атомов Н атомами хлора – гексахлорбензол С6Сl6 – фунгицид; его применяют для сухого протравливания семян пшеницы и ржи против твердой головни. Продукт присоединения хлора к бензолу – гексахлорциклогексан (гексахлоран) С6Н6Сl6 – инсектицид; его используют для борьбы с вредными насекомыми. Упомянутые вещества относятся к пестицидам – химическим средствам борьбы с микроорганизмами, растениями и животными. Стирол C6H5 – CH = CH2 очень легко полимеризуется, образуя полистирол, а сополимеризуясь с бутадиеном – бутадиенстирольные каучуки. Применение бензола: полистирол Тренажеры Тренажер №1: “Способы получения гомологов бензола” Тренажер №2: “Уравнения реакций, иллюстрирующие химические свойства бензола” Тренажер №3: “Физические свойства бензола” Тренажер №4: “Химические свойства гомологов бензола” |
Поиск
Архив записей
Друзья сайта
Статистика
Онлайн всего: 1 Гостей: 1 Пользователей: 0 |
||||||||||||||||||||||||||||||||||||||||||||