Персональный сайт
Ростовцевой Ларисы Геннадьевны
учителя химии МБОУ Боханской СОШ № 2
|
Меню сайта
Наш опрос
Погода
|
Спирты: химические свойства, получение, применениеСпирты: химические свойства, получение, применениеХимические свойства спиртов В химических реакциях гидроксисоединений возможно разрушение одной из двух связей:
Это могут быть реакции замещения, в которых происходит замена ОН или Н, или реакция отщепления (элиминирования), когда образуется двойная связь. Полярный характер связей С–О и О–Н способствует гетеролитическому их разрыву и протеканию реакций по ионному механизму. При разрыве связи О–Н с отщеплением протона (Н+) проявляются кислотные свойства гидроксисоединения, а при разрыве связи С–О – свойства основания и нуклеофильного реагента.
С разрывом связи О–Н идут реакции окисления, а по связи С–О – восстановления. Таким образом, гидроксисоединения могут вступать в многочисленные реакции, давая различные классы соединений. Вследствие доступности гидроксильных соединений, в особенности спиртов, каждая из этих реакций является одним из лучших способов получения определенных органических соединений. 1. Кислотно-основные свойства RO- + H+ ↔ ROH ↔ R+ + OH- алкоголят-ион Кислотные свойства уменьшаются в ряду, а основные возрастают: HOH → R-CH2-OH → R2CH-OH → R3C-OH вода первичный вторичный третичный 1. Кислотные свойства Взаимодействие с активными щелочными металлами: Видео-опыт: “Взаимодействие этилового спирта с металлическим натрием” 2C2H5OH + 2 Na → 2C2H5ONa + H2 этилат натрия Алкоголяты подвергаются гидролизу, это доказывает, что у воды более сильные кислотные свойства C2H5ONa + H2O ↔ C2H5OH + NaOH 2. Основные свойства Взаимодействие с галогенводородными кислотами: Видео-опыт: “Взаимодействие этилового спирта с бромоводородом” C2H5OH + HBr H2SO4(конц)↔ C2H5Br + H2O бромэтан
Лёгкость протекания реакции зависит от природы галогенводорода и спирта – увеличение реакционной способности происходит в следующих рядах:
2. Окисление 1). В присутствии окислителей [O] – K2Cr2O7 или KMnO4 спирты окисляются до карбонильных соединений: Видео-опыт: “Окисление этилового спирта раствором перманганата калия” Видео-опыт: “Окисление этилового спирта кристаллическим перманганатом калия” Видео-опыт: “Каталитическое окисление этанола” Видео-опыт: “Окисление этанола (тест на алкоголь)” Первичные спирты при окислении образуют альдегиды, которые затем легко окисляются до карбоновых кислот.
При окислении вторичных спиртов образуются кетоны.
Третичные спирты более устойчивы к действию окислителей. Они окисляются только в жестких условиях (кислая среда, повышенная температура), что приводит к разрушению углеродного скелета молекулы и образованию смеси продуктов (карбоновых кислот и кетонов с меньшей молекулярной массой). В кислой среде: Для первичных и вторичных одноатомных спиртов качественной реакцией является взаимодействие их с кислым раствором дихромата калия. Оранжевая окраска гидратированного иона Cr2O72- исчезает и появляется зеленоватая окраска, характерная для иона Cr3+ . Эта смена окраски позволяет определять даже следовые количества спиртов. CH3- OH + K2Cr2O7 + 4H2SO4 → CO2 + K2SO4 + Cr2(SO4)3 + 6H2O 3CH3-CH2-OH + K2Cr2O7 + 4H2SO4 → 3CH3COH + K2SO4 + Cr2(SO4)3 + 7H2O В более жёстких условиях окисление первичных спиртов идёт сразу до карбоновых кислот: 3CH3-CH2-OH + 2K2Cr2O7 + 8H2SO4 t→ 3CH3COOH + 2K2SO4 + 2Cr2(SO4)3 + 11H2O Третичные спирты устойчивы к окислению в щелочной и нейтральной среде. В жёстких условиях (при нагревании, в кислой среде) они окисляются с расщеплением связей С-С и образованием кетонов и карбоновых кислот. В нейтральной среде: CH3 – OH + 2KMnO4 →K2CO3 + 2MnO2 + 2H2O, а остальные спирты до солей соответствующих карбоновых кислот. 2). Качественная реакция на первичные спирты Видео-эксперимент:“Окисление этилового спирта оксидом меди (II)”
Видео-опыт: “Качественная реакция на этанол”
Видео-опыт: “Качественная реакция на многоатомные спирты”
3). Горение (с увеличением массы углеводородного радикала – пламя становится всё более коптящим) CnH2n+1-OH + O2 t → CO2 + H2O + Q
Видео-опыт: “Горение спиртов” 3. Реакции отщепления 1) Внутримолекулярная дегидратация CH3-CH2-CH(OH)-CH3 t>140,H2SO4(к)→ CH3-CH=CH-CH3 + H2O бутанол-2 бутен-2
В тех случаях, когда возможны 2 направления реакции, например: Дегидратация идет преимущественно в направлении I, т.е. по правилу Зайцева – с образованием более замещенного алкена. Правило Зайцева: Водород отщепляется от наименее гидрированного атома углерода соседствующего с углеродом, несущим гидроксил.
2) Межмолекулярная дегидратация 2C2H5OH t<140,H2SO4(к)→ С2H5-O-C2H5 + H2O простой эфир При переходе от первичных спиртов к третичным увеличивается склонность к отщеплению воды и образованию алкенов; уменьшается способность образовывать простые эфиры. 3) Реакция дегидрирование и дегидратация предельных одноатомных спиртов –реакция С.В. Лебедева 2C2H5OH 425,ZnO,Al2O3→ CH2=CH-CH=CH2 + H2 + 2H2O 4. Реакции этерификации Спирты вступают в реакции с минеральными и органическими кислотами, образуя сложные эфиры. Реакция обратима (обратный процесс – гидролиз сложных эфиров). Получение спиртов 1. В промышленности 1. Из водяного газа (получение метанола – древесный спирт) CO + 2H2 t,p → CH3OH 2. Брожение глюкозы (получение этанола) C6H12O6 дрожжи → 2C2H5OH + 2CO2 3. Гидратация алкенов
2. В лаборатории Взаимодействие галогеналканов R-Г с водными растворами щелочей CH3Cl + NaOH t, водн.р-р.→ CH3OH + NaCl (р. обмен) Применение
Тренажеры Тренажер №1: “Химические свойства предельных одноатомных спиртов” Тренажер №2: “Способы получения предельных одноатомных спиртов” |
Поиск
Архив записей
Друзья сайта
Статистика
Онлайн всего: 1 Гостей: 1 Пользователей: 0 |


















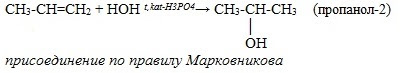
 Метанол СН3ОН – используют как растворитель, в производстве муравьиной кислоты, а также в производстве формальдегида, применяемого для получения фенолформальдегидных смол, в последнее время метанол рассматривают как перспективное моторное топливо. Большие объемы метанола используют при добыче и транспорте природного газа. Метанол – наиболее токсичное соединение среди всех спиртов, смертельная доза при приеме внутрь – 100 мл.
Метанол СН3ОН – используют как растворитель, в производстве муравьиной кислоты, а также в производстве формальдегида, применяемого для получения фенолформальдегидных смол, в последнее время метанол рассматривают как перспективное моторное топливо. Большие объемы метанола используют при добыче и транспорте природного газа. Метанол – наиболее токсичное соединение среди всех спиртов, смертельная доза при приеме внутрь – 100 мл. Этанол С2Н5ОН – исходное соединение для получения ацетальдегида, уксусной кислоты, а также для производства сложных эфиров карбоновых кислот, используемых в качестве растворителей. Кроме того, этанол – основной компонент всех спиртных напитков, его широко применяют и в медицине как дезинфицирующее средство.
Этанол С2Н5ОН – исходное соединение для получения ацетальдегида, уксусной кислоты, а также для производства сложных эфиров карбоновых кислот, используемых в качестве растворителей. Кроме того, этанол – основной компонент всех спиртных напитков, его широко применяют и в медицине как дезинфицирующее средство.














